Les bactériophages (également dénommés phages) sont des virus qui infectent spécifiquement les bactéries. Ils ont été décrits pour la première fois par un chercheur anglais, Frederick Twort, en 1915. Deux ans après et de manière indépendante, Felix d’Hérelle, un chercheur Franco-Canadien fit également la découverte des bactériophages. Il envisagea immédiatement leur utilisation pour éliminer des bactéries pathogènes et traiter des infections. Il est ainsi considéré comme le précurseur de la phagothérapie (la thérapie par les phages). Puisque ces virus sont capables de tuer une espèce de bactérie, pourquoi ne pas les utiliser pour éliminer une bactérie pathogène? C’est la base de la phagothérapie qui est utilisée actuellement dans de nombreux pays de l’Est. En Europe de l’Ouest des recherches ont récemment démarré afin de valider cette thérapie selon les normes de nos instances de santé publique.
Chaque type de phages reconnait une espèce, voir une sous-espèce de bactérie. Un bactériophage ne va donc pas infecter et éliminer toutes les bactéries mais uniquement celles qui vont être reconnues par le phage et permettre sa multiplication. De par sa grande spécificité, un bactériophage ne pourra jamais infecter une de nos propres cellules.
Présents dans l’ensemble de la biosphère, les bactériophages constituent l’entité biologique la plus répandue et la plus diversifiée sur Terre. On estime leur nombre à 1031 sur la planète. Ils jouent un rôle environnemental essentiel, notamment en régulant la croissance bactérienne mais également en contribuant à l’évolution génétique de nombreux micro-organismes. L’étude des bactériophages a contribué au développement de nos connaissances du vivant et à l’essor de la biologie moléculaire. Actuellement, avec l’émergence de souches bactériennes résistantes aux antibiotiques, les phages sont considérés comme une alternative plus que prometteuse aux antibiothérapies classiques.
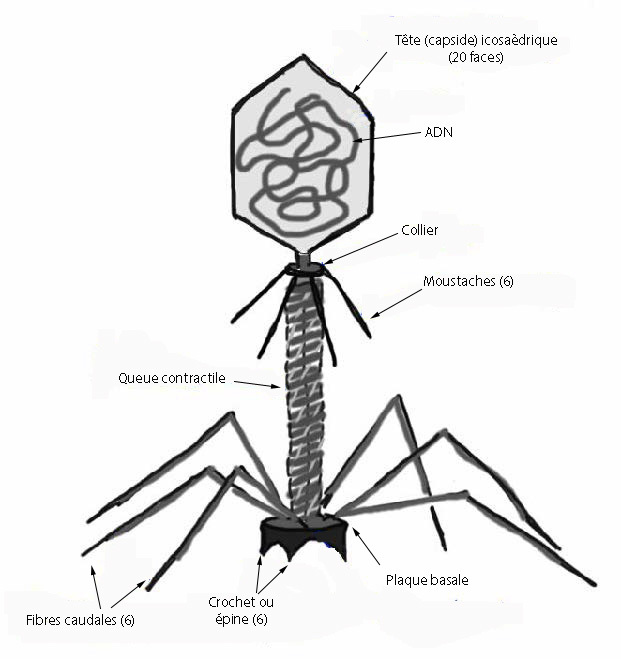
Lorsqu’un bactériophage est en présence d’une bactérie hôte, il va se fixer sur des récepteurs spécifiques situé à la surface de la bactérie: c’est l’adsorption. Le virus va alors injecter son ADN à l’intérieur de la bactérie. Celui-ci va détourner la machinerie bactérienne qui va devenir une usine à fabriquer des bactériophages. Une centaine de virus sera ainsi produit par la bactérie qui va finir par lyser pour laisser sortir les bactériophages. Ceux-ci vont pouvoir ainsi infecter les autres bactéries hôtes. C’est ce que l’on nomme le cycle lytique.
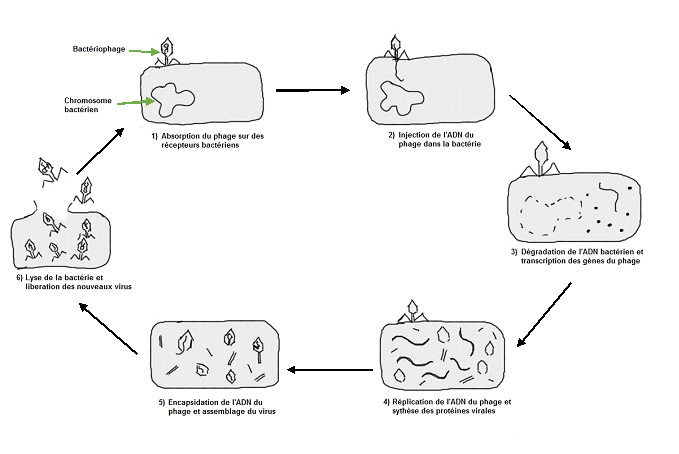
Certains types particuliers de bactériophages sont également capables d’intégrer leur matériel génétique dans le génome de la bactérie hôte. On parle alors de phages lysogènes. La bactérie hôte ne sera pas lysée mais son génome va contenir et exprimer des gènes du phage. Ceux-ci peuvent coder pour de dangereuses toxines. Certaines souches d’E. coli ou le Vibrio cholera, par exemple, deviennent pathogènes grâce à l’ADN d’un phage intégré dans leur génome. En conditions défavorables pour la bactérie, le phage lysogène redevient lytique.
L’expérience proposée va permettre de mettre en évidence des bactériophages de l’environnement capables de lyser une souche d’E. coli. Des ressources pédagogiques (liens en bas du protocole) permettront à l’enseignant d’aller plus loin dans la discussion avec sa classe en parlant de l’importance et de l’abondance des bactériophages dans l’environnement ainsi que de la phagothérapie comme complément aux antibiotiques.
Protocole :
Note: Afin de faire tenir l'expérience en classe sur 2 séances, les manipulations du JOUR1 peuvent être effectuées par l'assistant.
JOUR 1
1) Prélèvement d’échantillons.
Là où il y a des bactéries, il y a des bactériophages ! Le plus simple est d’effectuer un prélèvement dans différents cours d’eau (Arves, Rhône, autres rivières ou fontaines à proximité de l’école). Il n’est pas nécessaire de faire un prélèvement héroïque au milieu du cours d’eau. Les bactéries et donc les phages, diffusent largement dans l’eau et un prélèvement depuis la berge fonctionne très bien. Plus le cours d’eau est « sale », plus il y a de chance d’avoir des bactériophages. L’Arve à la jonction est facile d’accès et contient de nombreux bactériophages. Un prélèvement en aval de la sortie d’une station d’épuration est également envisageable.
- Plonger un tube 50 ml dans l’eau et le remplir.
- Fermer le tube et noter la provenance de l’échantillon sur le tube.
NOTE: Il est important de récupérer l'eau le jour même ou la veille de l'expérience. Au delà, les résultats ne sont pas garantis.
2) Elimination des bactéries de l’échantillon
Les bactéries ne passent pas à travers les filtres d’une porosité de 0.45 μm. En revanche les bactériophages, plus petits passent à travers.
- Filtrer environ 20 ml de l’échantillon d’eau dans un nouveau tube 50 ml (noté F). Attention à travailler stérilement.
Pour cela Il est important de retirer le piston avant de mettre le filtre pour ne pas le déchirer. Puis le filtre est ajouté à l’extrémité de la seringue. L’eau est ensuite versée dans la seringue et le piston inséré délicatement. Appuyer délicatement pour filtrer l’eau. Une pression trop forte risque de décrocher le filtre.
3) Enrichissement en bactériophages
- Prélever 9 ml du filtrat (tube F) et les transférer dans un nouveau tube 50 ml (noté E). Le reste peut être utilisé par un autre binôme. Garder les ml de filtrat (tube F) restants à 4°C. Ils seront utilisés plus tard.
Les 9 ml ne contiennent plus de bactérie mais peuvent contenir des bactériophages contre E. coli.
- Ajouter 1 ml de milieu de culture concentré (LB 10x) aux 9 ml d’eau filtrée.
A l’aide d’une anse stérile prélever un peu d’E. coli et la resuspendre dans les 10 ml de solution.
- Fermer le tube
- Incuber le tube à 37°C 24h
E. coli va se multiplier grâce au milieu de culture. Si un ou plusieurs phages capables d’infecter E. coli sont présents dans les 9 ml de l’échantillon d’eau, ils vont l’infecter et s’y multiplier (enrichissement). Après 24h un nombre suffisant de bactériophages pourra est mis en évidence.
Après cette période d’incubation, le tube peut être gardé 1 semaine à 4 °C
JOUR 2
4) Mise en évidence des bactériophages
- Filtrer le milieu d’enrichissement délicatement comme décrit au point 2) en récupérant le filtrat dans un tube de 15 ml (noté EF).
Cette étape permet d’éliminer E. coli qui n’a pas été lysée par les éventuels bactériophages
Le filtrat (tube EF) peut être gardé à 4°C. Les bactériophages sont relativement stables et la préparation peut être conservée au moins une année dans ces conditions
- Faire une suspension d’E. coli (la même souche qu’utilisée pour l’enrichissement des phages (point 3 du protocole) comme effectué au point 2 mais en resuspendant cette fois-ci E. coli dans 5 ml d’eau physiologique stérile
- Imbiber un écouvillon stérile avec la suspension. Essorer légèrement contre la paroi du tube et frotter l’écouvillon sur une boîte de pétri. Il est important d’effectuer des stries serrées afin de déposer des bactéries sur toute la boîte en grande quantité. Répéter l’opération en tournant la boîte d’un tiers pour strier dans une autre direction. Répéter une troisième fois l’opération en tournant encore la boîte d’un tiers.
Cette manipulation est identique à l’étalement effectué pour l’expérience No 15 : les antibiotiques. Il s’agit ici d’obtenir un « gazon » bactérien.
- Laisser sécher la boite quelques minutes
- Noter au dos de la boite les numéros ou noms des échantillons qui vont être déposé
- Déposer 5 μl de l’enrichissement filtré (tube EF).
- Déposer 5 μl de l’eau filtrée non enrichie (tube F)
- Déposer 5 μl d’une suspension de bactériophage T4 spécifique contre E. coli (contrôle positif)
- Déposer 5 μl d’eau physiologique stérile (contrôle négatif)
- Il est également possible de déposer 5 μl d’enrichissement (EF) d’autres échantillons
- Laisser sécher la boite quelques minutes sans la secouer. Quand la goutte de 5 μl a complètement disparue, incuber la boite à l’envers à 37 °C de 12 à 24 h.
- La boite peut être conservée ensuite à 4°C
JOUR 3
5) Résultat
- Observer les plages de lyse
- Conclure sur la présence ou non de bactériophages contre E. coli
- Si E. coli était une souche pathogène, discutez du concept de phagothérapie
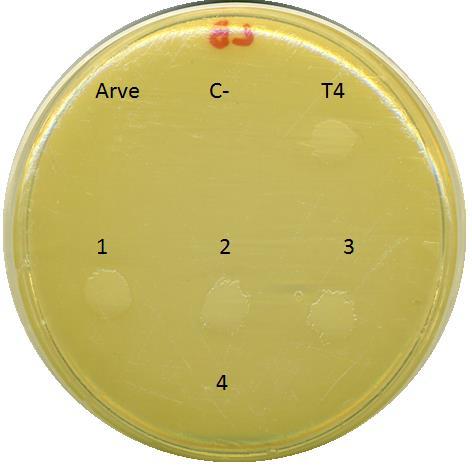
| Arve : eau de l’Arve filtrée (sans enrichissement) ; C- : eau physiologique stérile ; T4 : suspension de phage T4 ; 1 à 4 : Différents échantillons d’eau après enrichissement : 1) eau de l’Arve (jonction); 2 eau de l’Arve (Quai E.- Ansermet) ; 3) eau de l’Arve (Carouge) ; 4) eau du Rhône (jonction). Aucun phage n’a été mis en évidence dans l’eau du Rhône. |
6) Pour aller plus loin
Une liste de films et de livres est donnée ici à titre indicatif pour aller plus loin autour de la phagothérapie. Certains DVD de films peuvent être mis à disposition par BiOutils.
Films-documentaires:
- Cent regrets M. d'Herelle (2013). Film Octopussyprod
Lien RDM video : http://www.rdm-video.fr/film-dvd/V61263/cent-regrets-m-d-herelle.html
- Bactéries résistantes: des virus au secours des malades (2013). Emission 36.9, RTS
Lien RTS : http://www.rts.ch/emissions/36-9/5102290-bacteries-resistantes-des-virus-au-secours-des-malades.html
- Virus contre bactéries: une solution à la crise des antibiotiques? (2011) Un film de Stefanie Schmidt.
Lien dailymotion: http://www.dailymotion.com/video/xocrd3_virus-contre-bacteries-une-solution-a-la-crise-des-antibiotiques_tech
- La guerre des phages (2005). Un film de Lindalee Tracey
Lien youtube : https://www.youtube.com/watch?v=nVD5tYE8oyI
Livres:
- La phagothérapie: des virus pour combattre les infections. Renouveau d'un traitement au secours des antibiotiques. 2017, Alain Dublanchet, Editions Favre (Français, 252 pages)

- Viruses vs superbugs: a solution to the antibiotics crisis? 2007, Thomas Hausler, Macmillan (anglais, 256 pages)

Et encore:
- Site web d'information sur la phagothérapie: phageback.ch et atelier pour les enseignants:https://wp.unil.ch/phageback/2015/09/phagotherapie-formation/
- Ateliers à L'Eprouvette (Lausanne): http://wp.unil.ch/mediationscientifique/2015/phageback-ateliers-debats/
- Références scientifiques: http://www.phagoburn.eu/
Cette expérience a été mise en place en collaboration avec Johan Roelant, Maria Gaulin et Carmen Diz Salgado du Collège Voltaire.
Matériel fourni:
- Micropipettes P20
- Micropipettes P1000
- Boîte de pointes jaunes
- Boîte de pointes bleues
- Seringue 20 ml
- Filtre 0.45 um
- Tubes plastique 50 ml
- Tubes plastique 15 ml
- Milieu LB 10x
- Bouteille d'eau stérile
- Ecouvillons
- Souche Escherichia coli
- Boîtes de Petri LA
- Anse d'inoculation
- Portoir tube 15/50 ml
Matériel non fourni:
L’Université de Genève décline toutes responsabilités en cas de dommages survenus durant les expériences.

